- Ciała stałe
- Piryt i ametyst
- Sprytna plastelina
- Topnienie lodu
- Stop Wooda
- Gazy
- Balonik na kolbie
- Balonik pod kloszem
- Termometr miłości
- Wrzenie wody pod zmniejszonym ciśnieniem
- Ciecze
- Naczynia połączone
- Naczynia kapilarne
- Tornado w butelce
- Ruch konwekcyjny
- Plazma
- Elektroskop i świeca
- Tornado ogniowe
- Lampa plazmowa
- Induktor
- Kondensat
Termometr miłości
Równowaga termodynamiczna oznacza, że taka sama ilość par skrapla się ile alkoholu paruje.
Obliczenie ciśnienia pary nasyconej w danej temperaturze to trudne zadanie. Dla wody ciśnienie to wynosi 1 atmosferę (czyli 1013 hPa) w temperaturze 100ºC (wrzenie wody oznacza, że ciśnienie pary wodnej w bąbelku jest równe ciśnieniu atmosferycznemu). W temperaturze 20ºC wynosi ono, ale 17/760 ciśnienia atmosferycznego (17 torr, czyli mm słupa rtęci – dawne jednostki) czyli 2% (stąd w meteorologii podaje się zawartość pary wodnej w atmosferze jako 0-4% wilgotności bezwzględnej). W temperaturze 0ºC ciśnienie nie wynosi wcale 0, ale 6,13 hPA - mniej niż jedna setna atmosferycznego: stąd chmury nawet na wysokościach kilkunastu kilometrów, gdzie temperatura wynosi do minus 55ºC.
Niżej przedstawiamy wyniki modelu numerycznego z niemieckiego przedsiębiorstwa chemicznego.
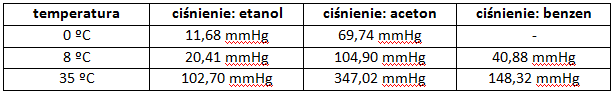
Ciśnienie pary nasyconej alkoholu jest niskie w temperaturze 0ºC (wynosi około 11,68 Tr – 11,68/760 atm) zmienia się silnie w zakresie temperatur 20-30ºC. Dlatego, koneserzy koniaków, lubią przed jego skosztowaniem potrzymać kieliszek w dłoni, tak aby koniak rozlany po ściankach trochę wyparował – ważny w koniaku jest i smak i zapach.
Ciśnienie benzenu w temperaturze 8ºC (temperatura zestalania się benzenu wynosi
-4,95
ºC) jest dość wysokie – aż 40,88
Tr: benzyna śmierdzi, nawet zimą.
Stosunkowo wysokie (aż 347,02
Tr) jest natomiast ciśnienie acetonu w temperaturze 35ºC: zmywacz do paznokci aż dusi (naprawdę dusi, jeśli zawiera aceton!)
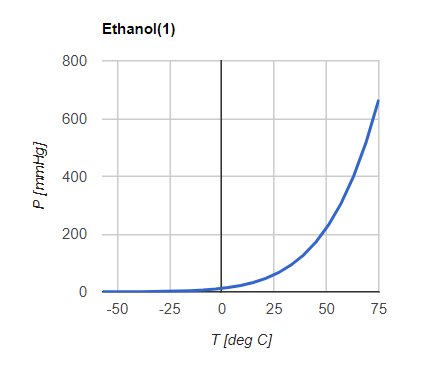
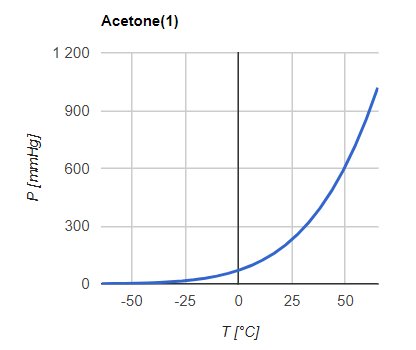
Rys. 2. Zależność ciśnienia od temperatury (ddbonline.ddbst.de)