 |
Start |
| JAK
ZOBACZYĆ ATOMY |
|
 |
Ruchy Browna |
 |
Młynek Crookesa |
 |
Doświadczenie Perrina |
 |
Mikroskop sił atomowych |
|
ELEKTRONY - PIERWSZE SKŁADNIKI ATOMÓW
|
|
 |
Wyładowania
w próżni |
 |
Promieniowanie katodowe, kanalikowe, lampa Thompsona |
 |
Lampa Brauna |
 |
Kula plazmowa |
 |
Doświadczenie Milikana |
| FIZYKA W KWANTACH |
|
 |
Ciało doskonale czarne |
 |
Źródła światła |
 |
Efekt fotoelektryczny |
 |
Bateria słoneczna, fotoogniwo |
| ATOM WODORU | |
| |
|
 |
Kolorowe płonienie |
 |
Rurki Plückera |
 |
Widmo ciągłe,
pasmowe, liniowe |
 |
Absorpcja |
| JĄDRO I JEGO SKŁADNIKI | |
| |
|
 |
Radioaktywność |
 |
Doświadczenie Rutheforda |
 |
Komora Wilsona |
 |
Kwarki |
| KOSMOLOGIA | |
 |
Soczewski grawitacyjne |
 |
Badania mgławic spiralnych |
 |
Pracowite panie |
 |
Edwin Hubble |
 |
Belgijski ksiądz i astronom |
 |
Wszechświat wg Einsteina |
 |
Tajemniczy szum |
 |
Rozdzielczość aparatury |
 |
Historia Wszechświata |
 |
Ostatnie odkrycia: supernowe |
 |
Składniki Wszechświata |
| FIZYKA W ZASTOSOWANIACH | |

|
Laser i diagram Jabłońskiego |
| Fizyka współczesna, Fizyka dla każdego, WFAiIS, UMK |
 Rura Crookesa – strumień elektronów pozostawia "cień" na szerszym końcu rury Plücker stwierdził,
że w rurkach do wyładowań przy ciśnieniach około miliona razy
mniejszych od ciśnienia atmosferycznego, przepływowi prądu
elektrycznego przez gaz towarzyszy zielonkawe świecenie rury szklanej,
w miejscach naprzeciw ujemnej elektrody - katody.
Wyglądało to tak, jakby katoda wysyłała jakieś nieznane promieniowanie, nazwane promieniowaniem katodowym.
W 1897 roku
„oficjalnie” przez J. J. Thompsona został odkryty elektron, a
dokładniej zmierzony stosunek e/m jego
ładunku e do masy m. Zastosowana
przez Thompsona metoda, odchylania wiązki elektronów przez pole
elektryczne i
magnetyczne jest stosowane w kineskopach telewizyjnych (tj.
odbiornikach TV
starszego typu). Metoda Thompsona stosowana jest nadal w spektrometrach
masowych, zob. poniżej, elektron zaś pozostaje jedną z niewielu
cząstek
naprawdę niepodzielnych. Nie są takimi niepodzielnymi cząstkami atomy
(Grecki a-tomos, czyli nie-podzielny),
z których potrafimy odłączyć elektrony. 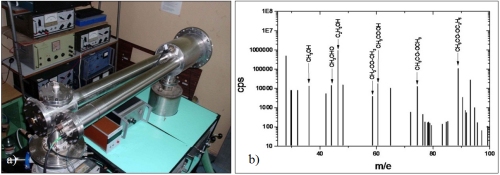 A) Spektrometr
masowy
pozwalający mierzyć ilość określonych związków chemicznych w zależności
od ich
masy (Pomorska Akademia Pedagogiczna, Słupsk; b) widmo
masowe „zapachu truskawek” – ilość zliczeń jonów w
zależności od stosunku ich masy do ładunku; najwięcej w tym zapachu
„zapachu”
jest alkoholu etylowego i kwasu octowego, ale sporo jest tez różnego
rodzaju
estrów, czyli aromatycznych związków powstających z kwasów organicznych
i
alkoholi (courtesy prof. D. Bassi, Uniwersytet Trento). |
