
Grażyna Kontrym-Sznajd
Instytut Niskich Temperatur i Badań Strukturalnych PAN, Wrocław
Epokowym odkryciem, które zmieniło oblicze medycyny,
początkując erę bezinwazyjnego obrazowania wnętrza ciała ludzkiego,
było odkrycie przez Wilhelma Röntgena tajemniczego promieniowania X.
Odkrycie to zostało dokonane zupełnie przypadkowo 8.11.1895 roku, w
czasie badań promieni katodowych w zaciemnionym laboratorium i w
obecności związków fluoryzujących. Fascynujące jest to, że w owych
czasach nawet nie wiedziano czym są promienienie katodowe - nie znano
elektronu, a za najmniejszą, niepodzielną cząstkę materii uważano (aż
do 1911 r.) atom (z greki átomos – niepodzielny). W tym czasie
promieniowanie katodowe, zatrzymywane przez obudowę lampy, traktowano
jako materię w stanie promienistym, natomiast na temat tajemniczych
promieni X (kiedy już uwierzono w ich istnienie) wysnuwano przeróżne
hipotezy – Rentgen podejrzewał, że są to fale eteru wypełniającego cały
Wszechświat. Jak się potem okazało, promieniowanie katodowe to strumień
elektronów emitowanych przez katodę, natomiast promienie X to fale
elektromagnetyczne generowane podczas wyhamowywania elektronów przez
anodę
(dokładne wyjaśnienie tego zjawiska podała dopiero mechanika kwantowa).
 |
Wilhelm Conrad Röntgen (27.03 1845 – 10.03.1923) fizyk niemiecki, laureat pierwszej Nagrody Nobla w dziedzinie fizyki (1901 r.) za odkrycie promieniowania X, nazwanego promieniowaniem rentgenowskim.Otrzymaną
Nagrodę Nobla Röntgen
w całości ofiarował Uniwersytetowi w Würzburgu, czego nie zrobił żaden
późniejszy laureat. Nie opatentował swojego wynalazku uważając, że: nauka to nie biznes, nauka powinna służyć ludzkości.
|
Rentgen, po 7 tygodniach intensywnych badań, kiedy miał już
pewność, że lampa Crookesa jest źródłem nie tylko promieniowania
katodowego, ale również niewidzialnych i niezwykle przenikliwych
promieni X, wykonał radiogram ręki żony i 28 grudnia 1895 r. złożył
pracę do druku, wysyłając również artykuł ze zdjęciami do kilku kolegów
w kraju i zagranicą. Część z nich uznała to za żart, inni doznali
szoku. Traf chciał, że profesor Exner z Wiednia pokazał zdjęcia grupie
młodych fizyków, wśród nich dr E. Lecherowi, którego ojciec był wydawcą
prasowym Vienna Presse. Dzięki temu już 5 stycznia 1896 r.
ukazała się w prasie wiedeńskiej informacja o odkryciu promieni X,
którą wkrótce przedrukowały czasopisma na całym świecie: Zamieszanie
spowodowane wojną nie powinno odwrócić uwagi od
wspaniałego triumfu nauki. Wiedeńdonosi, że prof.
Röntgen z Uniwersytetu w Würzburgu odkrył światło, które
pozwala wykonywać otografie przez drewno, ciało ludzkie,
ubranie i większość innych substancji organicznych.
Profesor zdołał sfotografować kawałki metalu zamknięte w
drewnianej skrzynce i otrzymał zdjęcie ręki ludzkiej, na
którym widoczne są tylko kości, bez tkanki mięśniowej”
(Londyn, Daily Chronicle, 6.01.1896 r.).
Niezwykle interesująca jest historia polskiej radiologii, a tempo jej rozwoju wręcz imponujące [4, 5]. Prawie natychmiast po ukazaniu się informacji na temat odkrycia Röntgena, profesor chemii Uniwersytetu Jagiellońskiego (UJ), Karol Olszewski, wykonał rentgenogramy różnych przedmiotów, o czym 21.01.1986 r. poinformowała krakowska gazeta CZAS. Wkrótce potem przeprowadzono pierwsze badanie radiologiczne (ramka 2).
|
|
Przedruk z ówczesnej gazety: zdjęcie trwało siedem kwadransów; ręka nieszczęśliwego objektu była za pomocą opasek z blachy przyśrubowana do stołu i w ten sposób unieruchomiona. |
Ramka 2 – pierwsze badanie radiologiczne w Polsce. Prof. chirurgii UJ, A. Obaliński, wykorzystał promienie X do zbadania łokcia górnika. Badanie wykonał prof. K. Olszewski z asystentami.
Mnie jednak, jako fizyka zajmującego się metodami tomografii
komputerowej, najbardziej zachwyciły prace polskiego lekarza, dr Karola
Mayer’a, który w lipcu 1914 r., na zjeździe we Lwowie, wygłosił
referat, przedstawiając metodę otrzymywania obrazów w oparciu o zasady
tomografii. Praca ta, mimo iż została opublikowana (ramka 3), uszła
uwadze światowej i wśród pomysłodawców tomografii komputerowej ten
genialny lekarz, który jest również autorem patentu lampy rtg,
zaopatrzonej w dwie lub więcej anod i katod (Patentschrift nr 274790) i
wielu innych wynalazków [6], nie jest wymieniany.
Pomysł Mayera wyprzedził o 7 lat przedstawienie idei trójwymiarowego
obrazowania przez A. Bocage oraz uzyskanie przez niego patentu w 1921
r. Tę datę przyjęto jako powstanie tomografii rentgenowskiej,
jakkolwiek jej prawdziwy rozwój zapoczątkowały dopiero prace Cormacka
[7] (teoria) oraz brytyjskiego inżyniera G. Hounsfield’a (konstrukcja
pierwszego tomografu z zastosowaniem promieni X – rys. 1), za
które obaj badacze otrzymali w roku 1979 Nagrodę Nobla
|
|
w czasie całej ekspozycyi wykonuję szybkie a małe ruchy lampą tam i na powrót, równolegle do osi podłużnej lub poprzecznej... Przez ten prosty sposób osiągam albo zupełne zniknięcie cieni, nie należących do cienia sercowego i naczyń głównych, albo częściowe oddzielenie się ich tak, że zoryentowanie się co do kształtu poszczególnych łuków staje się możliwem. (publ. 1916 r.) |


Tomografia (z greckiego: tomé + gráfein) oznacza
przekrój + zapisywać. Idea Cormacka była następująca. Obiekt „kroimy”
na wzajemnie równoległe płaszczyzny, „zbierając dane”, a następnie
przeprowadzając rekonstrukcję obrazu, na każdej z tych płaszczyzn
niezależnie (rys. 2). Z jednej strony obiektu umieszczone jest źródło
promieni X o natężeniu I0 , z
drugiej strony odbiornik, rejestrujący natężenie tego promieniowania po
przejściu przez obiekt wzdłuż danej linii L. Zmiana natężenia
tego promieniowania zależy od gęstości w każdym z punktów r znajdujących
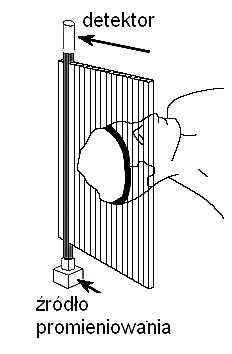
się na wybranej linii L. Wykonując pojedyncze zdjęcie rentgenowskie
(rtg) otrzymujemy obraz (rys. 2), na którym każdy punkt na kliszy
odpowiada jednemu równaniu o wielu niewiadomych. Jeżeli jednak
prześwietlimy obiekt pod wieloma kątami (nawet zmieniając kąt co 10 w zakresie od 0 do 1800),
otrzymamy dodatkowe równania, co pozwala odtworzyć gęstość w dowolnym
punkcie r. Na tej zasadzie pracowały tomografy pierwszej
generacji.
 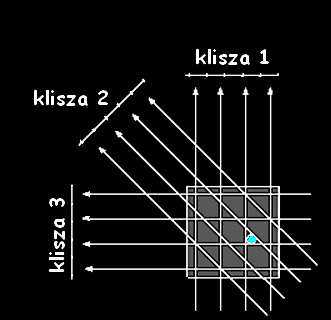 |
Rys. 2. Tomografia to wykonanie
serii „zdjęć” - prześwietlenie obiektu pod wieloma kątami. Dzielenia
obiektu na płaszczyzny wzajemnie równoległe pozwala sprowadzić
rekonstrukcję trójwymiarowego obrazu do zespołu dwuwymiarowych
rekonstrukcji.
|
Matematycznych metod tomografii komputerowej jest bardzo wiele – od
rozwiązywania równań algebraicznych, poprzez transformaty Fouriera do
różnorodnych rozwiązań tzw. transformaty Radona [9]. Metody te są
ciągle udoskonalane, tak jak i aparatura badawcza (rys. 3), dzięki
czemu otrzymywany obraz jest coraz lepszej jakości, a przy okazji
napromieniowanie pacjenta mniejsze.
Ponieważ tomografia rtg1 pozwala jedynie zróżnicować tkanki o odpowiednio różnej gęstości, co nie zawsze daje możliwość odróżnienia zmian patologicznych od fizjologicznych, następuje szybki rozwój innych metod diagnostycznych, takich jak emisyjna tomografia pozytonowa (PET, 1975 r.) i magnetyczny rezonans jądrowy (NMR, 1977 r.) – rys. 3.
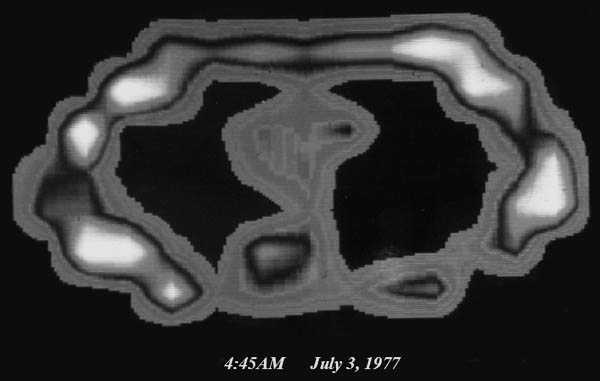
 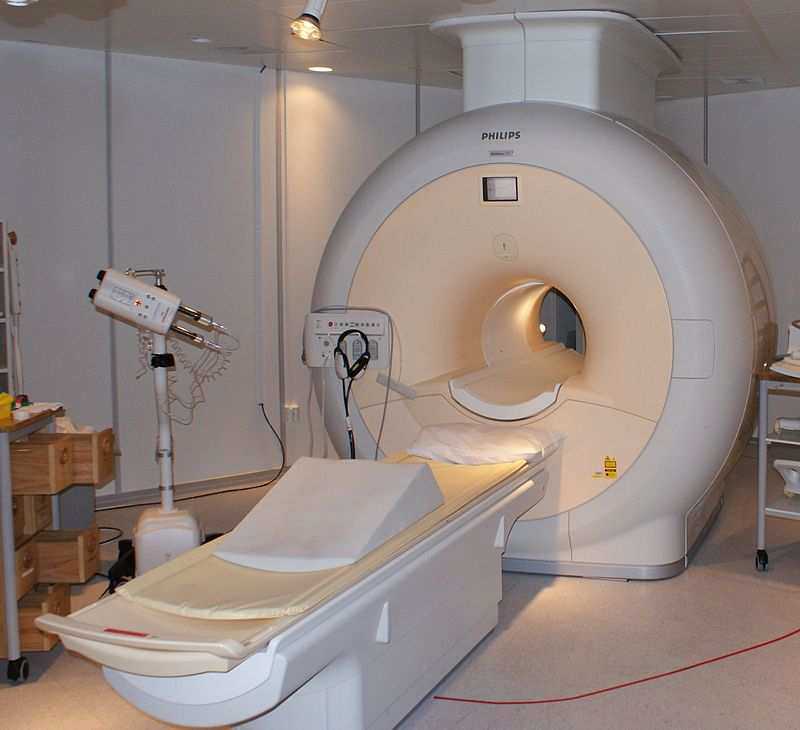 Rys. 3. Aparatura NMR i obrazy otrzymywane kiedyś i dziś. Pierwszy udany skan NMR zarejestrowano już w lipcu 1977 r. (źródło) |
 |
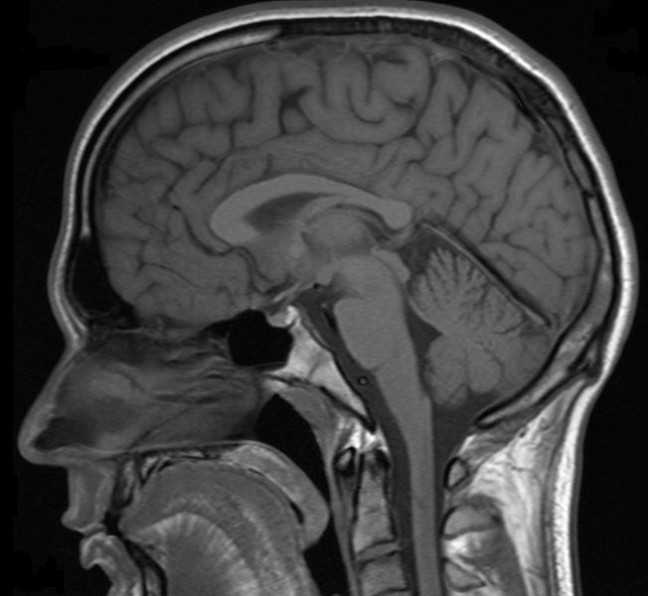 |
Magnetyczny rezonans jądrowy to zjawisko absorpcji
a następnie, w wyniku powrotu układu do stanu równowagi, rejestracji
re-emisji fal elektromagnetycznych (o częstotliwości radiowej) przez
jądra atomowe (o niezerowym spinie) znajdujące się w stałym polu
magnetycznym. Niezerowy spin maja jądra o nieparzystej liczbie
nukleonów, takie jak 1H,13C, 15N, 17O, 19F, 23Na, 31P. Częstość
rezonansowa zależy od pola magnetycznego jak i konkretnego
jądra – w ten sposób można „wybierać” rezonans na określonych jądrach,
którymi najczęściej są protony, czyli jądra wodoru. Stosowanie
dodatkowo środków kontrastowych, mających różne właściwości
magnetyczne, pozwala badać funkcje narządów, jak np. wydzielanie
nerkowe, ogniska zapaleń, ukrwienie. śeby odtworzyć obraz jak w
tomografii, częstość rezonansowa musi być funkcją położenia – dlatego
stałe pole magnetyczne posiada gradient (w funkcji położenia) w jednym,
dwóch, a nawet trzech kierunkach. Największe znaczenie ma NMR w
badaniach kręgosłupa oraz angiografii, tzn. uzyskiwaniu obrazu naczyń
krwionośnych. W badaniach naukowych stosuje się też czynnoś- ciowy NMR,
badając najczęściej aktywność neuronów podczas odbierania różnych
bodźców.
Tomografia pozytonowa oparta jest na zjawisku anihilacji elektronu i
pozytonu (antycząstki elektronu), prowadzącym do zamiany ich masy na
energię, emitowaną w postaci kwantów gamma. Jeżeli w procesie
anihilacji nie bierze udziału żaden dodatkowy układ fizyczny, z zasady
zachowania pędu i energii wynika, że muszą powstać co najmniej dwa
fotony rozchodzące się prawie antyrównolegle. W związku z tym, jeżeli
liczniki rejestrujące liczbę powstających kwantów usytuujemy
antyrównolegle, tuż przy badanym obiekcie, zarejestrują one wszystkie
akty anihilacji, jakie zaszły na danej linii L.
Emisyjna2 tomografia
pozytonowa powstała na bazie autoradiografii tkanek, czyli rejestracji
rozmieszczenia preparatu promieniotwórczego w określonych narządach. W
badaniu tym stosuje się izotopy pierwiastków biogennych (naturalnych
pierwiastków występujących w organizmie ludzkim), których czasy
połowicznego rozpadu są na tyle krótkie [15O
(2,07 min), 13N (9,97 min), 11C (20,3 min), 18F (109.7
min.)], żeby napromieniowanie pacjenta było jak
najmniejsze. PET służy do badania przepływu krwi przez określone
narządy, ekspresji wybranych receptorów lub metabolizmu niektórych
substancji (tlenu, glukozy, leków, itd.), znakowanych preparatem
promieniotwórczym. Umożliwia to badanie czynnościowe narządów, zarówno
w obserwacjach stanów fizjologii, jak i patologii. Badania fizjologii,
gdzie wykorzystuje się ścisłe powiązania pomiędzy aktywnością
neuronalną, zużyciem energii i miejscowym przepływem krwi, dotyczą w
szczególności badania procesów zachodzących w mózgu, m.in. procesów
postrzegania, słuchania, myślenia i percepcji obrazów [10 – 12],
zilustrowanych na rys. 4.
|
|
Rys. 4. Aktywność mózgu kolejno dla słyszenia, wypowiadania oraz tworzenia wyrazów |
Do badania stanów patologicznych metodę PET wykorzystuje się w
neurologii, neurochirurgii, psychiatrii, kardiologii i onkologii (80%
wszystkich badań). W dziedzinie neurologii można zróżnicować przyczyny
otępienia, będącego objawem wielu chorób, np. choroby Alzheimera.
Badanie PET ma duże znaczenie w określeniu ognisk epileptycznych, co
decyduje o kwalifikacji pacjentów do zabiegu operacyjnego, jak również
umożliwia precyzyjne wykonanie operacji neurochirurgicznych. Kolejna
grupa schorzeń to choroby neurologiczne związane z zaburzeniami ruchu,
jak np. choroba Parkinsona. W celu oszacowania wydolności mięśnia
sercowego bada się metabolizm kwasów tłuszczowych, a dla lokalizacji
zawału - miejscowy przepływ krwi.
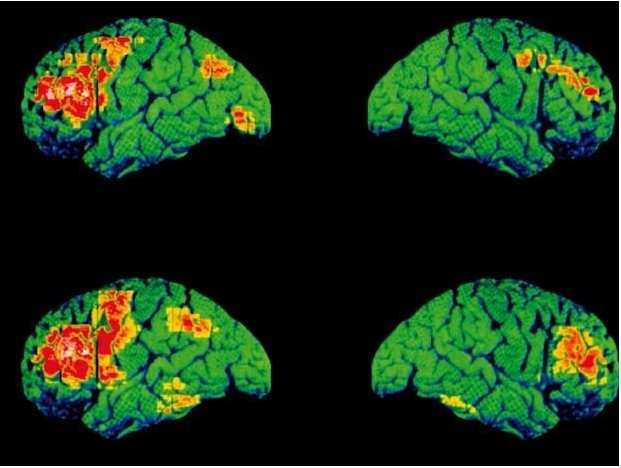 |
Rys. 5. Badanie aktywności mózgu
osoby mówiącej: osoby zdrowej i cierpiącej na schizofrenię (prawa i
lewa część rysunku) (źródło) |
Metoda PET ma jednak największe znaczenie w onkologii, gdzie wykorzystuje się zależność metabolizmu glukozy od stopnia uzłośliwienia nowotworu, pozwalającą odróżnić zmianę łagodną od złośliwej, stwierdzić przerzuty czy odróżnić nawrót guza od zmiany powstałej wskutek operacji, chemio- lub radioterapii. Badanie PET ma istotne znaczenie w momencie trudności diagnostycznych - w takim przypadku wykonanie badania całego ciała umożliwia umiejscowienie procesu nowotworowego. Na rys. 6 przedstawiono wyniki badania pacjenta z nowotworem mózgu: NMR stwierdza istnienie cysty, natomiast PET pokazuje te obszary, w których zwiększony metabolizm glukozy świadczy o złośliwości guza.
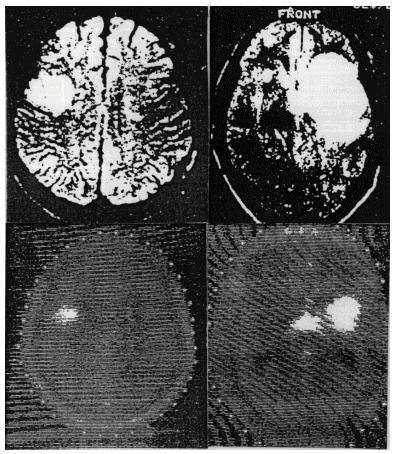 |
Rys. 6. Astrocytoma, st. złośliwości II. Górna część rysunku przedstawia wyniki NMR, dolna wyniki PET [13]. |
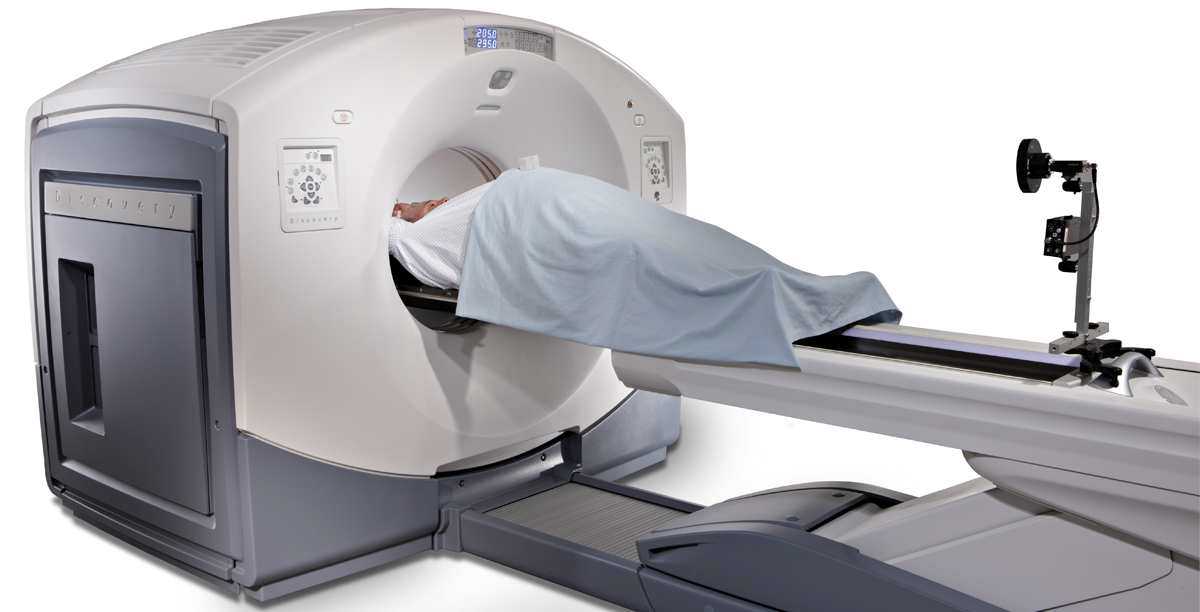
Może ucieszy nas fakt, że najnowocześniejszy skaner PET-CT GE
Discovery
IQ, który skraca czas badania z 20 do 4 minut i zapewnia precyzyjny
obraz drobnych zmian nowotworowych, uruchomiono we Wrocławiu. Aparatura
ta (rys. 7) pozwala wykonać do tysiąca badań miesięcznie (koszt jednego
wynosi 3 300 zł), lokalizując zmiany nowotworowe wielkości 2-3 mm
(aparatura poprzedniej generacji wykrywała ogniska chorobowe 5-6 mm). W
czerwcu 2015 r. taką aparaturę uruchomiono również w Poznaniu.
Rys. 7. Skaner PET-CT GE Discovery IQ, którego „światowa premiera” odbyła się 12.2014 r. w USA, jest pierwszym takim aparatem w Polsce i czwartym w Europie (informacja z marca 2015 r.). |
 |
Znane i popularne badanie scyntygraficzne (rejestracja fotonu
emitowanego przez źródło promieniotwórcze umieszczone w ciele pacjenta)
może być również przeprowadzone w technice trójwymiarowego obrazowania.
Jest to tomografia pojedynczego fotonu, SPECT (skrót od single-photon
emission computed tomography), mająca szerokie
spektrum zastosowań klinicznych. W przeciwieństwie do skanera PET,
który jest zazwyczaj używany do obrazowania całego ciała z
wykorzystaniem 18F-fluorodeoksyglukozy, w badaniu SPECT, używając
różnych radiofarmaceutyków, bada się zazwyczaj konkretny organ, np.
tarczycę po podaniu jodu 131. Technika ta, rozwijana od lat 70., będąca
znacznie tańszą od obrazowania PET, również w ostatnich latach przeżywa
„rewolucję technologiczną”.
Postęp technologiczny powoduje powstawanie (i to w coraz
krótszych odstępach czasu, ostatnio nawet 2-3 lat) sprzętu kolejnej
generacji - dotyczy to zarówno ulepszania istniejących aparatur
badawczych jak i powstawania nowych metod diagnostycznych. Najnowszy
rodzaj badań z zastosowaniem metod tomografii komputerowej to optyczna
koherentna tomografia, OCT (Optical Coherence Tomography) – pierwszy
tomogram żywego oka wykonano w 2001 roku. Wykorzystując interferencję
wiązek światła o długości zbliżonej do podczerwieni, rozproszonej na
warstwach oka, przeprowadza się badanie (z rozdzielczością 0.01 - 0.02
mm) siatkówki w obrębie plamki żółtej, nerwu wzrokowego oraz rogówki,
tęczówki i soczewki.
W ostatnich latach powstała również 3-wymiarowa (a nawet 4-wymiarowa,
gdzie czwartym wymiarem jest czas) technologia USG. Jest ona niezwykle
przydatna w położnictwie, ponieważ obserwacja narządów wewnętrznych
płodu zwiększa wykrywalność jego wad.
Tomografia ma wielorakie zastosowanie, również w badaniach
materiałowych. Stosowane są tu dwa rodzaje mikrotomografów rtg:
micro-CT (dokładność do 1 m = 10-3 mm)
oraz nano- CT (1 nm=10-6 mm), które
pozwalają badać szczegóły o rozmiarach 200 nm (sto razy mniejszych niż
włos). Micro-CT stosowane są m.in. w geologii, architekturze, rzeźbie i
budownictwie (do badania zjawiska wietrzenia, konserwacji kamienia
budowlanego); jubilerstwie (analizy czystości kamieni szlachetnych),
itd. Nano-CT pozwoli m.in. poznać strukturę kości, np. w celu
zaprojektowaniu idealnej i trwałej endoprotezy.
Dzięki tomografii rtg, w Gabonie odnaleziono jednocentymetrowe
struktury, skomplikowane wielokomórkowe formy życia sprzed 2 miliardów
lat (rys. 8), które poprzedzają aż o 1,5 mld lat "eksplozję kambryjską"
[14]. Legendarny „Betts”, stradivarius z 1704 r., został
zrekonstruowany - pracami kierował radiolog z amerykańskiej kliniki.
Jak się okazało, instrument ma swoją wewnętrzną anatomię [15].
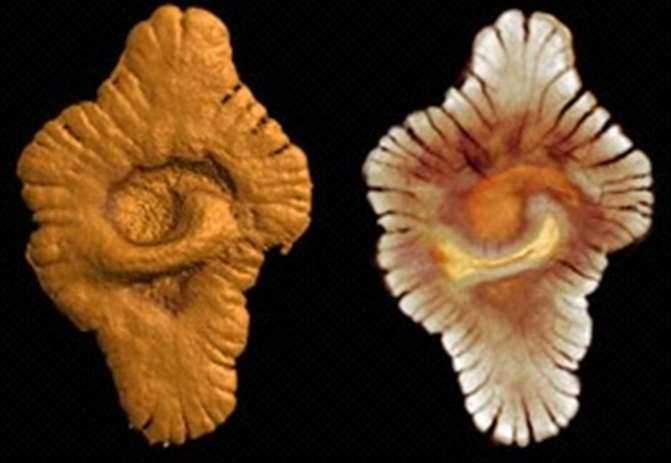 |
Rys. 8. Znaleziska w Gabonie [14]. |
Na zakończenie powrót do Krakowa, na UJ, gdzie grupa fizyków, pod kierownictwem prof. Pawła Moskala, prowadzi badania nad udoskonaleniem aparatury PET, nazwanej J-PET (Jagiellonian Positron Emission Tomograph) [16].
|
|
Rys. 9. Grupa fizyków z UJ przy zestawie nowych liczników do aparatury J- PET. |
Badania prowadzone w tym zakresie doczekały się już 12 patentów
jak również wyróżnienia złotym medalem na Światowych Targach
Wynalazczości, Badań Naukowych i Nowych Technologii: BRUSSELS INNOVA
2009. Prowadzone prace maja na celu uruchomienie nowej aparatury,
wykorzystującej organiczne materiały scyntylacyjne (rys. 9). Pozwoli to
istotnie obniżyć koszt aparatury PET jak również zwiększyć efektywność
i szybkość odtwarzania obrazu (również dzięki obrazowaniu całego ciała)
[17]. Ponadto, tego typu aparatura zostanie wykorzystana do badań
„struktury” różnorodnych materiałów porowatych, mających unikalne
zastosowania, m.in. jako „magazyny” różnych substancji, w tym leków. Z
kolei biomateriały o odpowiedniej strukturze mogą służyć do otrzymania
analogów tkanek naturalnych a nawet do stworzenia medycznych
mikrorobotów [18].
1
z
niezrozumiałych powodów
potocznie nazywana CT (computer tomography), ponieważ NMR i PET to
również tomografie komputerowe. Spotykane nazwy, np. PET-CT oznaczają,
że połączono dwie metody diagnostyczne – w tym przypadku PET i
tomografię rtg.
2 Tomografia
emisyjna, w odróżnieniu od transmisyjnej,
jaką jest NMR oraz CT, oznacza, że źródło promieniowania znajduje się
wewnątrz badanego obiektu.